【問題】
【難易度】★☆☆☆☆(易しい)
次の文章は,銅の電解精製に関する記述である。文中の\( \ \fbox{$\hskip3em\Rule{0pt}{0.8em}{0em}$} \ \)に当てはまる最も適切なものを解答群の中から選びなさい。
電線で用いられる高純度の銅は,熱化学的に得られた粗銅を電解精製による一段のプロセスで,不純物濃度を\( \ \fbox { (1) } \ % \ \)以下に小さくして作られる。この高純度化によって銅は柔軟性が増すと共に\( \ \fbox { (2) } \ \)が小さくなる効果があり,電解精製は実用的には欠かすことができない。銅の電解精製では硫酸が電解液として用いられ,粗銅は\( \ \fbox { (3) } \ \)としての機能をもつ。この電解液中で銅は\( \ \fbox { (4) } \ \)イオンとして存在し,これが還元されて高純度の銅が得られる。銅の電解精製プロセスでは銅のもつ溶解電位,又は析出電位を利用するが,簡単には元素のもつイオン化傾向の差を用いると考えてよい。この際,生成する銅の質量はファラデーの電気分解の法則に従い,用いた電気量に比例する。ここでファラデー定数が用いられる。ファラデー定数は電子素量と\( \ \fbox { (5) } \ \)の積である。具体的には有効数字\( \ 3 \ \)桁で表して\( \ 96500 \ \mathrm {C / mol} \ \)が使われることが多い。
〔問4の解答群〕
\[
\begin{eqnarray}
&(イ)& カソード &(ロ)& 反応電子数 &(ハ)& 電気抵抗 \\[ 5pt ]
&(ニ)& 1 &(ホ)& 10 &(ヘ)& 反応モル数 \\[ 5pt ]
&(ト)& 0.1 &(チ)& -2価 &(リ)& アボガドロ数 \\[ 5pt ]
&(ヌ)& アノード &(ル)& 電気伝導性 &(ヲ)& 隔 膜 \\[ 5pt ]
&(ワ)& 1 価 &(カ)& 展 性 &(ヨ)& 2 価 \\[ 5pt ]
\end{eqnarray}
\]
【ワンポイント解説】
高校生の化学の延長のような問題です。高校生の頃,化学をしっかり勉強されていた方であれば難なくとれるかもしれません。高校の頃を思い出す意味でもよく理解するようにして下さい。
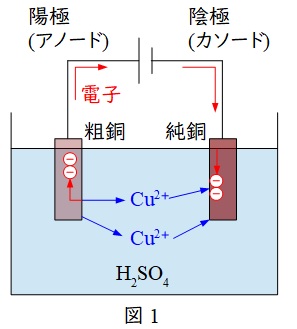
1.銅の電解精製プロセス
図1に示すようなプロセスとなり,陽極と陰極の酸化還元反応にて,陰極に銅を析出させ,銅の純度を上げることができます。
\[
\begin{eqnarray}
陽極(アノード)&:& \mathrm {Cu} &→& \mathrm {Cu}^{2+} +2\mathrm {e}^{-} \\[ 5pt ]
陰極(カソード)&:& \mathrm {Cu}^{2+} +2\mathrm {e}^{-} &→& \mathrm {Cu} \\[ 5pt ]
\end{eqnarray}
\]
【解答】
(1)解答:ト
題意より,解答候補は(ニ)\( \ 1 \ \),(ホ)\( \ 10 \ \),(ト)\( \ 0.1 \ \)になると思います。電線で用いられる銅はできるだけ高純度の銅が理想であり,\( \ 99.9 \ % \ \)以上の純度すなわち\( \ 0.1 \ % \ \)以下の不純物濃度で作られます。
(2)解答:ハ
題意より,解答候補は(ハ)電気抵抗,(ル)電気伝導性,(カ)展性,になると思います。展性は打撃や圧力にてどこまで破壊されることなく広げられるかという意味で,電気伝導性,展性共に純度が上がると大きくなります。電気抵抗は不純物濃度が下がると小さくなります。
(3)解答:ヌ
題意より,解答候補は(イ)カソード,(ヌ)アノード,になると思います。ワンポイント解説「1.銅の電解精製プロセス」の通り,粗銅の反応は陽極(アノード)の反応となります。
(4)解答:ヨ
ワンポイント解説「1.銅の電解精製プロセス」の通り,銅はイオン化すると\( \ \mathrm {Cu}^{2+} \ \)となり,2価の陽イオンとなります。
(5)解答:リ
ファラデー定数\( \ F \ \)は電気素量\( \ e=1.6022\times 10^{-19} \ \)とアボガドロ数\( \ N_{\mathrm {A}}=6.0221\times 10^{23} \ \)の掛け算となり,
\[
\begin{eqnarray}
F&=& e\times N_{\mathrm {A}} \\[ 5pt ]
&=& 1.6022\times 10^{-19}\times 6.0221\times 10^{23} \\[ 5pt ]
&≒& 96486 → 96500 \ \mathrm {C / mol} \\[ 5pt ]
\end{eqnarray}
\]
で求められます。






















 愛知県出身 愛称たけちゃん
愛知県出身 愛称たけちゃん