Contents
【問題】
【難易度】★★★☆☆(普通)
次の文章は,電気化学システムに関する記述である。文中の\( \ \fbox{$\hskip3em\Rule{0pt}{0.8em}{0em}$} \ \)に当てはまる最も適切な語句を解答群の中から選びなさい。
電気エネルギーと化学エネルギーの直接変換を担う電気化学システムは,基本構成として電子伝導体である二つの電極とイオン伝導体である電解質とから構成されている。この二つの電極はアノードとカソードと呼ばれ,各々役目が異なる。アノードでは\( \ \fbox { (1) } \ \)反応が起こり,電気分解の際には\( \ \fbox { (2) } \ \)極となる。電解質としては酸又はアルカリの水溶液がよく知られており,鉛蓄電池では\( \ \fbox { (3) } \ \)水溶液が用いられている。電気化学システムには室温付近で運転するものに限らず,高温のシステムもある。\( \ 1000 \ \mathrm {[℃]} \ \)付近で運転するアルミニウム電解においては,高温でのイオン性融体である\( \ \fbox { (4) } \ \)が利用されている。
以上の電極,電解質といった基本要素のほか,二つの電極系の分離や二つの電極の接触防止のために両極間に\( \ \fbox { (5) } \ \)が用いられることもある。
〔問7の解答群〕
\[
\begin{eqnarray}
&(イ)& 陽 &(ロ)& 固体電解質 &(ハ)& 還 元 \\[ 5pt ]
&(ニ)& アルカリ &(ホ)& カソード &(ヘ)& 酸 化 \\[ 5pt ]
&(ト)& 硫 酸 &(チ)& カソライト &(リ)& 塩 酸 \\[ 5pt ]
&(ヌ)& セパレータ &(ル)& アノライト &(ヲ)& 中 和 \\[ 5pt ]
&(ワ)& 陰 &(カ)& 溶融塩 &(ヨ)& 食 塩 \\[ 5pt ]
\end{eqnarray}
\]
【ワンポイント解説】
化学エネルギーと電気エネルギーの変換を行う電気化学システムに関する問題です。
正極・負極,酸化・還元,アノード・カソード等頭の中がごちゃごちゃになってしまうところですが,きちんと整理して覚えるようにしましょう。
1.鉛蓄電池
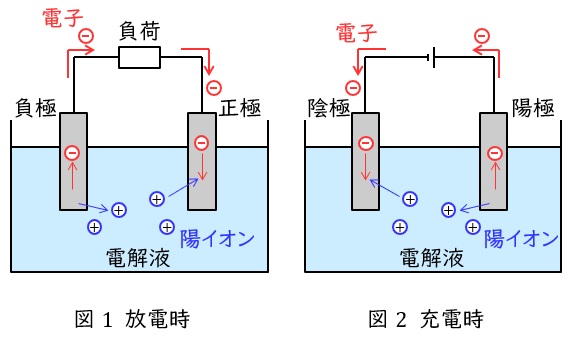
代表的な二次電池(蓄電池)の一つで,電解質に希硫酸を使用し,正極では鉛原子の価数が\( \ 4 \ \)の\( \ \mathrm {PbO_{2}} \ \)から価数が\( \ 2 \ \)の\( \ \mathrm {PbSO_{4}} \ \)に変わる還元反応,負極では鉛原子の価数が\( \ 0 \ \)の\( \ \mathrm {Pb} \ \)から価数が\( \ 2 \ \)の\( \ \mathrm {PbSO_{4}} \ \)に変わる酸化反応となります。
酸化反応を生じる電極をアノード,還元反応を生じる電極をカソードといいます。
①反応式(放電時,充電時は逆)
\[
\begin{eqnarray}
正極&:& \mathrm {PbO_{2}} &+& \mathrm {{SO_{4}}^{2-}} &+& \mathrm {4H^{+}} + \mathrm {2e^{-}} &→& \mathrm {PbSO_{4}} &+& \mathrm {2H_{2}O } \\[ 5pt ]
負極&:& \mathrm {Pb} &+& \mathrm {{SO_{4}}^{2-}} && &→& \mathrm { PbSO_{4}} &+& \mathrm {2e^{-} } \\[ 5pt ]
\hline
全体&:& \mathrm {Pb} &+& \mathrm {PbO_{2}} &+& \mathrm {2H_{2}SO_{4}} &→& \mathrm {2PbSO_{4}} &+& \mathrm {2H_{2}O } \\[ 5pt ]
\end{eqnarray}
\]
2.溶融塩電解
イオン化傾向の大きいナトリウム\( \ \left( \mathrm {Na}\right) \ \),マグネシウム\( \ \left( \mathrm {Mg}\right) \ \),アルミニウム\( \ \left( \mathrm {Al}\right) \ \)等の金属は電気分解を行っても負極に析出することができず水素が発生してしまうため,金属塩を高温で溶解した溶融塩で電気分解を行うことで析出させます。
アルミニウム電解においては,溶融した氷晶石\( \ \left( \mathrm {Na_{3}AlF_{6}}\right) \ \)にアルミナ\( \ \left( \mathrm {Al_{2}O_{3}}\right) \ \)を加えて電気分解することで陰極に液体のアルミニウムが得られます。
(以下参考)
\[
\begin{eqnarray}
反応式: 2\mathrm {Al_{2}O_{3}} + 3\mathrm {C} → \mathrm {4Al} + \mathrm {3CO_{2}} \\[ 5pt ]
\end{eqnarray}
\]
※イオン化傾向
大きい方から順に,\(\mathrm {K}\),\(\mathrm {Ca}\),\(\mathrm {Na}\),\(\mathrm {Mg}\),\(\mathrm {Al}\),\(\mathrm {Zn}\),\(\mathrm {Fe}\),\(\mathrm {Ni}\),\(\mathrm {Sn}\),\(\mathrm {Pb}\),\(\mathrm {( H )}\),\(\mathrm {Cu}\),\(\mathrm {Hg}\),\(\mathrm {Ag}\),\(\mathrm {Pt}\),\(\mathrm {Au}\)(覚え方:かそうかな,まああてにすな,ひどすきるしゃっきん)
【解答】
(1)解答:ヘ
題意より解答候補は,(ハ)還元,(ヘ)酸化,(ヲ)中和,等になると思います。
ワンポイント解説「1.鉛蓄電池」の通り,アノードでは酸化反応が起こります。
(2)解答:イ
題意より解答候補は,(イ)陽,(ワ)陰,等になると思います。
ワンポイント解説「1.鉛蓄電池」の通り,電気分解の際に酸化反応が起こるのは陽極となります。
(3)解答:ト
題意より解答候補は,(ロ)固体電解質,(ト)硫酸,(リ)塩酸,(ヨ)食塩,等になると思います。
ワンポイント解説「1.鉛蓄電池」の通り,鉛蓄電池で電解質として使用されるのは硫酸水溶液となります。
(4)解答:カ
題意より解答候補は,(カ)溶融塩,(ヨ)食塩,等になると思います。
ワンポイント解説「2.溶融塩電解」の通り,アルミニウム電解においては溶融塩が用いられています。
(5)解答:ヌ
題意より解答候補は,(ヌ)セパレータ,等になると思います。
鉛蓄電池でも設けられますが,二つの電極系の分離や二つの電極の接触防止のために両極間にセパレータが用いられることがあります。












 【令和8年度版2種一次試験】
【令和8年度版2種一次試験】








 愛知県出身 愛称たけちゃん
詳しくは
愛知県出身 愛称たけちゃん
詳しくは