Contents
【問題】
【難易度】★★★★☆(やや難しい)
次の文章は,鉛蓄電池に関する記述である。
鉛蓄電池は,正極と負極の両極に\( \ \fbox { (ア) } \ \)を用いる。希硫酸を電解液として初充電すると,正極に\( \ \fbox { (イ) } \ \),負極に\( \ \fbox { (ウ) } \ \)ができる。これを放電すると,両極とももとの\( \ \fbox { (ア) } \ \)に戻る。
放電すると水ができ,電解液の濃度が下がり,両極間の電圧が低下する。そこで,充電により電圧を回復させる。過充電を行うと電解液中の水が電気分解して,正極から\( \ \fbox { (エ) } \ \),負極から\( \ \fbox { (オ) } \ \)が発生する。
上記の記述中の空白箇所(ア)~(オ)に当てはまる組合せとして,正しいものを次の(1)~(5)のうちから一つ選べ。
\[
\begin{array}{cccccc}
& (ア) & (イ) & (ウ) & (エ) & (オ) \\
\hline
(1) & 鉛 & 硫酸鉛 & 二酸化鉛 & 水素ガス & 酸素ガス \\
\hline
(2) & 鉛 & 二酸化鉛 & 硫酸鉛 & 水素ガス & 酸素ガス \\
\hline
(3) & 硫酸鉛 & 鉛 & 二酸化鉛 & 水素ガス & 酸素ガス \\
\hline
(4) & 硫酸鉛 & 二酸化鉛 & 鉛 & 酸素ガス & 水素ガス \\
\hline
(5) & 二酸化鉛 & 硫酸鉛 & 鉛 & 酸素ガス & 水素ガス \\
\hline
\end{array}
\]
【ワンポイント解説】
鉛蓄電池に関する問題で,前半が鉛蓄電池の反応,後半が水の電気分解の反応に関する問題となっています。
それぞれの内容をしっかりと化学反応式が書ける程度まで理解していれば解けますが,電験の問題としてはやや難しめの問題であったかもしれません。
1.鉛蓄電池
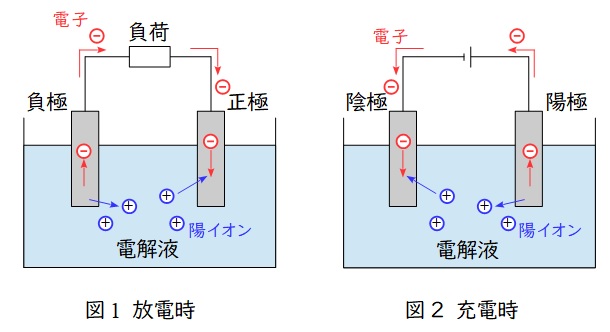
代表的な二次電池(蓄電池)の一つで,正極と負極では以下のような反応となります。
正極では鉛原子の価数が\( \ 4 \ \)の\( \ \mathrm {PbO_{2}} \ \)から価数が\( \ 2 \ \)の\( \ \mathrm {PbSO_{4}} \ \)に変わる還元反応,負極では鉛原子の価数が\( \ 0 \ \)の\( \ \mathrm {Pb} \ \)から価数が\( \ 2 \ \)の\( \ \mathrm {PbSO_{4}} \ \)に変わる酸化反応となります。
①反応式(放電時,充電時は逆)
\[
\begin{eqnarray}
正極&:& \mathrm {PbO_{2}} &+& \mathrm {{SO_{4}}^{2-}} &+& \mathrm {4H^{+}} + \mathrm {2e^{-}} &→& \mathrm {PbSO_{4}} &+& \mathrm {2H_{2}O } \\[ 5pt ]
負極&:& \mathrm {Pb} &+& \mathrm {{SO_{4}}^{2-}} && &→& \mathrm { PbSO_{4}} &+& \mathrm {2e^{-} } \\[ 5pt ]
\hline
全体&:& \mathrm {Pb} &+& \mathrm {PbO_{2}} &+& \mathrm {2H_{2}SO_{4}} &→& \mathrm {2PbSO_{4}} &+& \mathrm {2H_{2}O } \\[ 5pt ]
\end{eqnarray}
\]
【解答】
解答:(4)
(ア)
ワンポイント解説「1.鉛蓄電池」の通り,鉛蓄電池は正極と負極の両方に硫酸鉛\( \ \left( \mathrm {PbSO_{4}}\right) \ \)を用いる電池です。
(イ)
ワンポイント解説「1.鉛蓄電池」の通り,正極では充電時に二酸化鉛\( \ \left( \mathrm {PbO_{2}}\right) \ \)が生成されます。
(ウ)
ワンポイント解説「1.鉛蓄電池」の通り,負極では充電時に鉛\( \ \left( \mathrm {Pb}\right) \ \)が生成されます。
(エ)
過充電により電解液中の水が電気分解すると,正極では以下の酸化反応が起き,酸素ガスが発生します。
\[
\begin{eqnarray}
\mathrm {2OH^{-}} &→& \mathrm {\frac {1}{2} O_{2} + H_{2}O + 2e^{-}} \\[ 5pt ]
\end{eqnarray}
\]
(オ)
過充電により電解液中の水が電気分解すると,負極では以下の還元反応が起き,水素ガスが発生します。
\[
\begin{eqnarray}
\mathrm {2H_{2}O + 2e^{-}} &→& \mathrm {H_{2} + 2OH^{-}} \\[ 5pt ]
\end{eqnarray}
\]






















 愛知県出身 愛称たけちゃん
詳しくは
愛知県出身 愛称たけちゃん
詳しくは